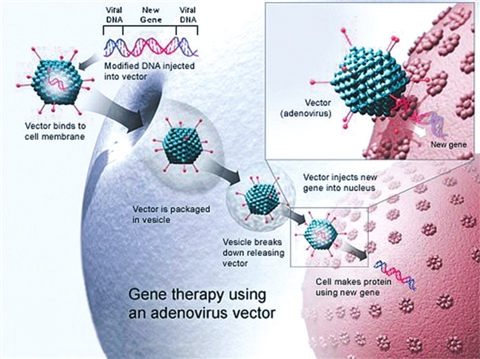
基因治疗
曙光重现
□本报记者 姚俊英
基因治疗的曲折历史
人类的某些疾病可以归因于人体自身基因的缺陷和环境或病原基因产物与人体的相互作用。也就是说,这些疾病都直接或间接地与基因有关,或者说它们属于基因功能缺陷的疾病。
基因治疗是将完好的基因转移至患者体内治疗疾病的一种方法。一般来说,基因治疗药物是一种预先构建好了的基因载体复合结构,只要它进入细胞后随机插入或定点整合(基因打靶)到染色体上,就能合成出该基因编码的正常蛋白质(酶)从而矫正原有突变基因合,成的异常蛋白质(酶)所导致的功能缺陷。
理论上,这样的策略不仅可用以治疗,还可治愈无数与遗传相关的人类疾
病。然而实际上,距离基因治疗的第一例人体试验已经过去20多年了,基因治疗尚未如大众希望的那样可以成为一种常态化的治疗手段。相反,1990自年以来,数以百计的临床试验都以失败告终,同时因为安全性问题,基因治疗一度陷入了泥潭。
开发安全有效的基因治疗并非易事。祁鸣说,基因治疗最早是从费城的一种免疫缺陷疾病开始的。此类患者缺乏正常运作的免疫系统,只能在类似于巨型气泡那样被完全隔离起来的高度无菌室环境下生活,以防止对普通人来说并不严重、对他们来说却可能造成致命的感染。临床试验开始时都进行得非常好:好几例病人成功
过上了正常的生活,不再局限于他们
的“气泡室”中。
但在几年之后,当时接受试验的20名患者中有5位患上了白血病,并且有一位不幸去世。
原因在哪里?一查,“ 原来是与运载矫正基因到体内骨髓细胞的逆转录病毒载体有关。载体进入细胞后到处乱跑,将正常工作的基因破坏了,细胞生长开始失控。祁鸣说。”
一系列事件令基因治疗产生了很大的负面作用。美国FDA开始意识到基因治疗可能具有潜在的、长期的副作用,大量基因治疗临床试验被搁浅,人们对于基因治疗的期望也跌入谷底,基因治疗开始沉默。
中外科学家的不懈探索
不过,基因治疗研究近几年情况开始出现好转。
虽然基因疗法并没有像15年或20年前人们的乐观预期那样发展迅速,但现在终于曙光初现。
说到基因治疗药物,祁鸣和记者都不约而同地想到了国内首个也是全球首个基因治疗药物“今又生”。
2004年1月,在外国科学家依然停留在数据收集或者动物试验阶段之时,中国深圳的赛百诺基因技术公司研发了用于治疗头颈部肿瘤的基因疗法药物――“重组人p53腺病毒注射液”并获,得了药监局的批准上市,其注册商标名为“今又生”。
但是,“今又生”由于 向药监局提交的申报材料中,仅有100余个临床试验病例,比美国食品药品监督管理局(FD A)审批某种新药所需的临床试验病例少得多,因此,事实上,“ 它并没有获得国外的肯定。祁鸣告诉记者。而国内”
许多三甲大医院也都持谨慎态度。今“又生”并没有获得预想的口碑和经济收益。
而在此之前,欧洲药物管理局以及美国食品药品监督管理局并未批准其他基因疗法药物的上市申请。因此,《NATURE》指出,次欧盟批准的此Glybera可谓掀开了基因治疗的新篇章。
据报道,Glybera用于治疗虽严格限制高脂肪饮食,却仍然发生了严重或反复胰腺炎发作的脂蛋白脂酶缺乏症(LPLD)患者。
研发该药的iuniQure公司在临床试验中,虽然仅仅邀请到27名患者参与试验,但这主要是因为该种病症的特殊性,患者数量本身并不多。考虑到这一因素,洲监管机构建议批准由荷兰欧uniQure公司研制和申报的基因治疗药物Glyber,并要求uniQure必须设立信息服务平台,通过注册表跟踪患者。
据介绍,LPLD是一种罕见的严重
遗传性疾病,目前无法治愈,发病率约为每百万人1~2例,在欧盟和北美受影响的患者数量仅有几百人。该疾病是由LP基因突变引起的,使患者LPL蛋白的活性严重下降或丧失。LPL蛋白是一种分解乳糜微粒的酶,如果乳糜微粒不被分解,就会在血液中积聚而堵塞小血管,从而可能导致复发性或严重急性胰腺炎。
“这相当于在你的血液中有10%的奶油。蒙特利尔大学教授丹尼尔 德特” ・(Daniel Gaudet)博士说。德特负责领导Glybera的临床试验。据悉,患有该病的人很容易得严重胰腺炎,除了采取严格限制高脂肪饮食措施外,目前还没其他治疗方法。但要患者坚持这样的严格饮食习惯并不容易,因此许多患者在胰腺炎发作时才住院。
如果使用该药,预计每位患者的花费将高达120万欧元(约合160万美元)将创造昂贵现代医药新纪录。,
承载重托造福人类
基因治疗虽然没有像人们当初预期的那样成为一场医学革命,但科学家们依然充满信心。对此,祁鸣也持相同观点。
祁鸣说,近年来基因治疗在一些领域取得突破性进展,也得益于各种基因技术的不断进步,以及多种基因载体的出现。
祁鸣向记者介绍了目前科学家发现的基因载体AAV(腺相关病毒)这个病,毒会固定在一个地方,不会到处乱跑。它没有毒性,不致病,宿主范围广,稳定性好。这也是迄今为止在许多疾病治疗
中应用最成功的载体。
但目前遇到的问题是,腺相关病毒这个“车”比较小,还没有一颗纳米粒子大。它所载的基因如果比较大的话,这个“车”就可能承载不了。因此,为了治疗更过的疾病,科学家可能在这方面还将继续探索与突破。据悉,目前还有腺病毒载体、慢病毒等多种基因载体出现。
不过,腺相关病毒载体对于一些眼部相关疾病,莱伯氏先天性黑蒙如(LCA,导致儿童失明的一种退行性视网膜疾病)倒是正好。同时,由于眼部是一个相对封闭的系统,因此,基因治疗手段相对比较安全,这也将为全世界数百万遗传性眼疾患者带来新的希望。
祁鸣告诉记者,费城的儿童医院已经使用此种基因病毒载体对患该种眼部疾病的儿童做了临床测试。他们先对一“只患有视网膜受损的狗进行基因治疗,取得了成功。之后开始对人进行临床测试,先对一只眼睛进行了治疗,大约已经有五六年的时间了,至少到目前还没有出现意外及后遗症。目前正在考虑对另一只眼睛进行治疗。据悉,目前全世界”已经成功开展了十几例这样的基因治疗手术。
而在去年,祁鸣和他的研究团队也宣布发现了一个新的莱伯氏先天性黑
蒙(Leber congenital amaurosis,LCA)致病 基 因 ――NMNAT1,并 首 次 将NMNAT1基因突变与人类疾病相关联起来,为罕见“黑蒙症”的基因诊断、治疗及药物开发提供了一条新途径。基“因治疗很关键的一点,就是我们必须知道一些疾病究竟是什么基因出了问题。祁鸣说。”
祁鸣告诉记者,前些天,一位巴西患者通过邮件联系他们,询问他们的研究进展,希望有朝一日能尽快进行基因治疗,恢复视力,重见光明。祁鸣预计,他们采用类似的基因治疗手段治疗这类先天性失明,等待的时间应该不会太长。
祁鸣说,基因治疗技术除了在遗传性失明领域已经大放异彩外,许多目前正在进行的其他基因治疗临床试验也都产生了积极的成果,这些试验治疗的疾病包括进行性肌不良、心肌病、艾滋病、血友病、神经退行性疾病、多种癌症等,而这些疾病在现阶段用其他医疗技术手段根本无法治愈。
据了解,由于载体的改良和技术的进步,这些试验没有一个出现了像基因治疗时代早期那样“打击”领域的毁灭性副作用,其中许多试验还产生了奇迹般的效果。